
Исследование этина

Докажем присутствие в этине (ацетилене) ненасыщенной
связи с помощью реактива Байера или бромной
воды. Для этого поместим реактив в пробирку и пропустим через него
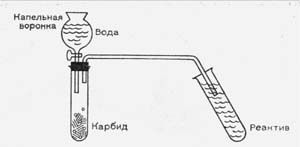
этин. Его мы получим в другой пробирке из нескольких кусочков карбида
кальция. Эту пробирку закроем резиновой пробкой с двумя отверстиями,
В одно из них заранее вставим стеклянную трубку с изогнутым концом
- он должен быть погружен в пробирку с реактивом. В другое отверстие
вставим капельную воронку и кран ее вначале закроем. Можно взять
вместо нее и простую стеклянную воронку, заменив кран зажимом, как
при получении метана. В воронку нальем воду
и, осторожно приоткрывая кран, будем медленно, по каплям, добавлять
ее к карбиду. Ввиду взрывоопасности этина проведем опыт вблизи от
открытого окна или в вытяжном шкафу. Вокруг ни в коем случае не
должно быть открытого пламени или включенных нагревательных приборов.
 Этин
в чистом состоянии представляет собой газ со слегка одурманивающим
запахом. Этин, полученный из технического карбида, всегда загрязнен
неприятно пахнущими ядовитыми примесями фосфористого водорода (фосфина)
и мышьяковистого водорода (арсина). Смеси этина с воздухом, содержащие
от 3 до 70 % этина, взрывоопасны. Этин очень легко растворяется
в ацетоне. В виде такого раствора его можно хранить и перевозить
в стальных баллонах. Этин
в чистом состоянии представляет собой газ со слегка одурманивающим
запахом. Этин, полученный из технического карбида, всегда загрязнен
неприятно пахнущими ядовитыми примесями фосфористого водорода (фосфина)
и мышьяковистого водорода (арсина). Смеси этина с воздухом, содержащие
от 3 до 70 % этина, взрывоопасны. Этин очень легко растворяется
в ацетоне. В виде такого раствора его можно хранить и перевозить
в стальных баллонах.
Этин можно превратить в очень многие соединения,
которые, в частности, приобрели большое значение для производства
пластмасс, синтетического каучука, лекарств и растворителей. Например,
при присоединении к этину хлористого водорода образуется винилхлорид
(хлористый винил) - исходное вещество для получения поливинилхлорида
(ПВХ) и пластмасс на его основе. Из этина же получают этаналь, с
которым мы еще познакомимся, а из него - многие другие продукты.
В будущем технология, основанная на применении карбида,
станет все больше вытесняться более выгодным нефтехимическим производство.
Главным недостатком карбидного метода получения этина является исключительно
большой расход электроэнергии.
|

![]()
![]()