
Фенопласты

К числу важнейших типов пластмасс, наряду с поливинилхлоридом,
полиэтиленом, полиамидами и полистиролом относятся также фенопласты
и аминопласты. Они принадлежат к группе реактопластов, т. е. таких
пластмасс, которые при нагревании не могут изменять свою форму.
Фенопласты и аминопласты получаются в результате поликонденсации.
Это такой процесс, при котором молекулы различных веществ соединяются
друг с другом и образуют макромолекулы, причем одновременно возникают
и другие, низкомолекулярные вещества - чаще всего вода. Хотя фенопласты-старейшая
разновидность пластмасс, они до сих пор отнюдь не устарели. В технологию
их получения все время вносятся отдельные усовершенствования, однако
в своей основе она не изменилась.
Изготовим прозрачную фенолоформальдегидную
смолу
В качестве исходных веществ возьмем 40%-ный водный
раствор метаналя (формалин) и кристаллический гидроксибен-зол (фенол)
или его метильные аналоги-крезолы. Если читателю не удастся найти
кристаллический фенол, можно использовать вместо него как можно
более концентрированный водный раствор фенола, то есть продажную
карболовую кислоту ("карболку"). Все названные вещества ядовиты!
Чтобы ознакомиться в общих чертах с процессом образования
смолы, смешаем в пробирке приблизительно 2 г кристаллического фенола
(или 4 мл раствора) с 3 мл формалина и добавим 3 капли концентрированной
соляной кислоты. При этом смесь самопроизвольно разогревается и,
наконец, закипает. Содержимое пробирки становится стеклообразным
и вязким. Тотчас стеклянной палочкой отберем пробу. При необходимости
немного охладим пробирку, чтобы реакция протекала не слишком бурно.
Взятую пробу реакционной массы испытаем на растворимость в воде
и спирте (денатурате) или других растворителях. Проба растворяется.
Тем временем реакция продолжается, содержимое пробирки становится
очень вязким и отчасти затвердевает (по консистенции напоминает
резину). Если теперь снова взять пробу, то она уже не растворяется,
но при нагревании еще проявляет пластичность. В конце опыта поставим
пробирку в химический стакан с кипящей водой. Через некоторое время
масса затвердевает. Разбив пробирку, мы можем достать из нее кусочек
прозрачной фенолоформальдегидной смолы. Она красноватая, не растворяется
и не плавится. При выдерживании в пламени смола сгорает очень медленно,
окрашивает пламя в желтый цвет, дает искры и обугливается. Горение
сопровождается интенсивным запахом фенола.
Попробуем теперь разобраться, какие химические реакции
происходят при выполнении этого опыта. Метаналь (формальдегид) имеет
атом кислорода при двойной связи. Этот атом вместе с двумя атомами
водорода фенола образует воду. За счет высвобождающихся при этом
единиц валентности появляется возможность присоединения молекул
фенола к остатку метаналя:
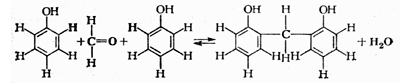
В этих реакциях участвует множество молекул, что
приводит к образованию цепей. Вначале возникают короткие цепи, и
полученный полимер представляет собой смолообраз-1;ое вязкое вещество,
легко растворимое, например в спирте и ацетоне (наша первая проба).
Этот полимер начальной стадии поликонденсации называют резолом.
Дальнейшее увеличение длины цепей приводит к тому, что вещество
почти полностью теряет свою растворимость в обычных растворителях
и проявляет пластичность только при нагревании (вторая проба). Продукт
этой стадии поликонденсации называется резитолом.
В конечном счете цепи соединяются между собой мостиками
из остатков метаналя и образуют трехмерную (пространственную) сетчатую
структуру:
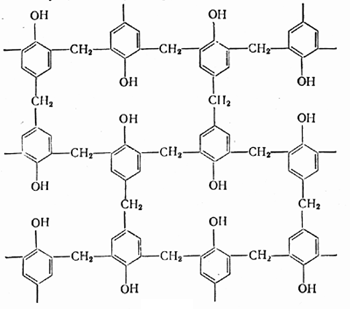
При этом полимер становится твердым, нерастворимым
V неплавким. Этот продукт конечной стадии поликонденсации называют
резитом.
При промышленной переработке смолу на стадии образования
резола выливают в формы и в них отверждают. Отверждение нередко
занимает несколько дней. Это необходимо для того, чтобы образующаяся
при реакции вода испарялась медленно. Иначе смола получится непрозрачной
и пузырчатой. Из литых фенолоформальдегидных смол изготовляют пуговицы,
рукоятки, бильярдные шары и т. д. Чтобы ускорить отверждение, можно
довести поликонденсацию почти до образования резита, затем полученную
смолу размолоть, поместить в формы, сжать под давлением 200-250
ат и подвергнуть отверждению при 160-170 °С. В последующих опытах
исследуем влияние на процесс поликонденсации различных условий.
Если мы будем проводить эту реакцию при рН выше 7, т. е. в щелочной
среде, то она сильно замедлится и ее можно будет остановить на стадии
образования резола.
|

![]()
![]()